近日,百洋医药集团、百洋众信基金投资企业同心医疗欧洲全资子公司BrioHealth BV宣布,公司自主研发的全磁悬浮植入式左心室辅助系统BrioVAD在欧洲的临床研究——BRIOLIFE试验,正式获得荷兰监管批准。荷兰是参与本次研究的欧洲国家中,首个批准开展试验的国家。BRIOLIFE试验将为欧洲晚期心衰治疗提供全新技术选择。

同心医疗BRIOLIFE临床研究是一项在欧洲开展的前瞻性、多中心、单组、基于预设目标值的非劣效性临床试验,旨在系统评估BrioVAD治疗晚期心衰患者的安全性与临床性能。该研究计划在欧洲12家临床中心开展,拟入组约60名患者,覆盖成人晚期心衰的短期及长期治疗,其主要终点为术后6个月生存率。
2024年底,同心医疗BrioVAD产品的美国INNOVATE临床试验正式获批,该研究作为与雅培HeartMate3开展的头对头大规模前瞻性随机对照研究,将为BrioVAD相较同类全磁悬浮产品的安全性和有效性评价,提供重要的高级别循证医学证据。在欧洲临床注册路径方面,同心医疗构建了更具前瞻性的全球化证据体系。
与业内普遍采用的单一区域临床数据申报CE认证模式所不同的是,公司拟采用“美国随机对照试验+欧洲前瞻性临床”双证据整合策略。后续欧洲BRIOLIFE临床研究的结果将与美国INNOVATE试验数据进行整合分析,形成综合临床评价报告,共同构成BrioVAD欧盟CE认证临床评价资料的核心组成部分,为BrioVAD进入欧洲市场提供更为全面、扎实的临床数据支撑。
此举有望树立欧洲心室辅助装置(VAD)市场准入新标杆,推动随机对照临床结果成为欧洲 VAD 产品准入的核心要求,引领欧洲市场行业监管升级。
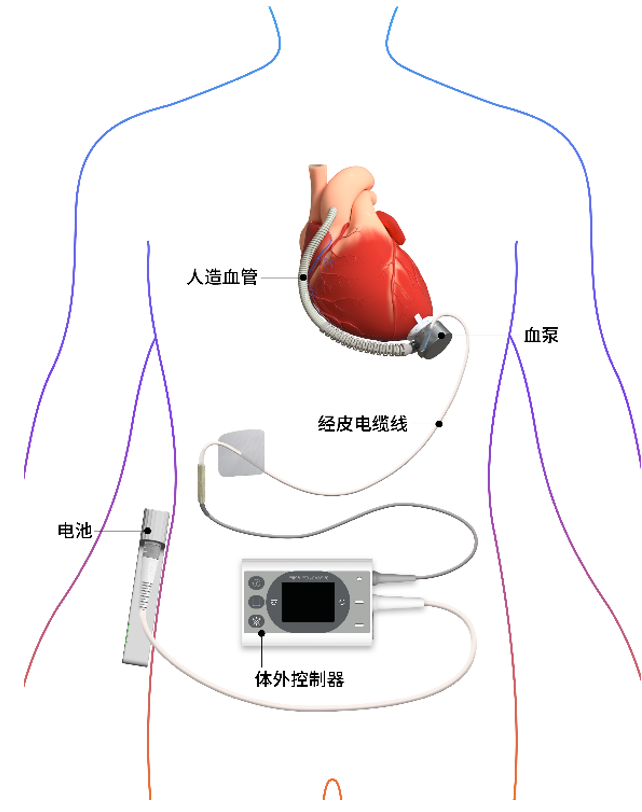
作为同心医疗面向全球市场开发的新一代全磁悬浮人工心脏,BrioVAD与已在中国实现商业化应用的CH-VAD采用相同植入式血泵。凭借国际首创的“分立式磁悬浮与电机设计”以及高度优化的流体力学设计,CH-VAD相较国际同类产品具备更小体积、更轻重量及更薄厚度,在降低血液损伤、减少溶血和血栓等并发症风险方面具备显著临床优势。此外,BrioVAD/CH-VAD采用全球数量最少(4根)、直径最细(3.3mm)的经皮电缆线,感染发生率处于全球公开报道较低水平。在患者日常使用体验方面,BrioVAD体外部件仅包含一块电池和一个控制器,轻便易携、操作简便,大幅提升患者日常活动与自主使用便捷性。
在美国市场,BrioVAD临床试验已取得令人振奋的进展。作为中国首个且唯一获得FDA批准在美国开展临床试验的有源植入式医疗器械,BrioVAD的INNOVATE临床研究,目前已完成超过200例患者植入,临床试验推进成效显著。与此同时,针对晚期心力衰竭儿科患者的Brio4Kids临床试验也已获得FDA附条件批准,进一步拓宽了产品的应用场景。
在中国市场,同心医疗通过引进国际先进的心衰治疗理念,和医学界合作,在中国开创和拓展了人工心脏疗法,并围绕植入患者全生命周期建立专业化服务体系,截至目前已完成超过800例CH-VAD植入,相关真实临床数据和使用经验不断积累,持续推动植入式人工心脏在国内临床应用的普及与发展,为更多国内晚期心衰患者带来生存希望。
在欧洲市场,除了已经获得荷兰监管批准外,BRIOLIFE临床试验申请也已获得德国、奥地利伦理委员会的批准,与5家欧洲临床中心完成试验协议签署,将在获批后同步启动临床研究工作。
随着BRIOLIFE欧洲临床研究稳步落地推进,同心医疗已初步构建起覆盖中国、美国、欧洲三大主流市场的国际化临床布局,全球化进程进入加速推进阶段。立足原创全磁悬浮技术优势,同心医疗将持续以不断突破的技术创新、扎实严谨的循证临床数据和国际标准的临床服务,为全球晚期心衰患者提供安全可靠的治疗方案,不断彰显中国高端医疗器械的全球创新实力与行业担当。
-
铸就中国民族制药新势力,青岛百洋制药生产车间及配套三期建设工程正式开工
2023-09-28 -
2023-02-27
-
百洋医药集团与昌平区政府签订战略合作协议,携手推进医药健康产业高质量发展
2023-03-03 -
百洋医药商业化平台又添新合作,再度携手安斯泰来共拓靶向药进口新篇章
2020-12-18 -
2021-06-30
-
百洋医药与北京门头沟区签署战略合作协议,科研成果转化基地全新启航
2022-04-18 -
2021-06-17
-
百洋医药商业化平台再添新伙伴,携手上海谊众共探肿瘤创新药物商业化
2022-02-14





